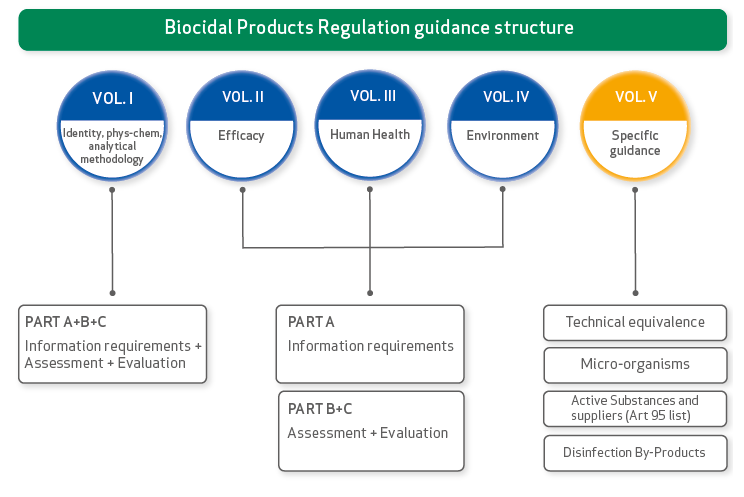
Volume I Identity/physico-chemical properties/analytical methodology
Parts A+B+C: Information Requirements, Assessment and Evaluation
This Guidance describes the information requirements for active substances and biocidal products in accordance with the Title 1 of Annex II and Annex III of the BPR, including technical advice on how to perform the hazard and exposure assessment and risk characterisation for biocidal active substances and products. (29/03/2022)
Volume II Efficacy
Part A: Information Requirements
This Guidance describes the information requirements for active substances and biocidal products in accordance with the Title 1 of Annex II and III of the BPR. (29/03/2022)
Parts B+C: Assessment and Evaluation
Guidance on the BPR: Volume II Efficacy, Assessment + Evaluation (Parts B+C). This Guidance provides technical advice on how to perform the hazard and exposure assessment and risk characterisation for biocidal active substances and products with respect to efficacy. (11/08/2023)
Volume III Human health
Part A: Information Requirements
This Guidance describes the information requirements for active substances and biocidal products in accordance with the Title 1 of Annex II and III of the BPR. (29/03/2022)
Parts B+C: Assessment and Evaluation
Guidance on the BPR: Volume III Human Health, Assessment + Evaluation (Parts B+C)
This Guidance provides technical advice on how to perform the hazard and exposure assessment and risk characterisation for biocidal active substances and products with respect to human health risk assessment and evaluation. (08/2025)
Part D: Dietary risk assessment and livestock exposure
Guidance on the BPR: Volume III Human Health, Dietary risk assessment and livestock exposure (Part D)
This Guidance provides technical advice on how to perform dietary risk assessment and livestock exposure assessment for biocidal active substances and products. This guidance is under revision and the currently valid version is the same as was provided in Vol III Parts B+C, version 4.0. (08/2025)
Volume IV Environment
Part A: Information Requirements
This Guidance describes the information requirements for active substances and biocidal products in accordance with the Title 1 of Annex II and III of the BPR. (29/03/2022)
Parts B+C: Assessment and Evaluation
This Guidance provides technical advice on how to perform the hazard and exposure assessment and risk characterisation for biocidal active substances and biocidal products with respect to environmental risk assessment. (25/10/2017)
Volume V Specific Guidance
Guidance to assess the risks to bees from the use of biocides
This Guidance provides technical advice on how to perform the hazard and exposure assessment and risk characterisation for biocidal active substances and biocidal products with respect to assessment of risks to bees from the use of biocides. (02/2024)
Guidance on Disinfection By-Products
This guidance document deals with the risk assessment for human health and the environment of Disinfection By-Products that is applicable for the authorisation of products under the EU Biocidal Products Regulation (BPR, Regulation (EU) 528/2012). (23/01/2017)
Guidance for identification of endocrine disruptors
This Guidance was developed jointly by ECHA and the European Food Safety Authority (EFSA) with support by the Joint Research Centre (JRC) and describes how to identify endocrine disruptors in the context of the Biocidal Products Regulation (EU) No 528/2012 and the Plant Protection Products Regulation (EC) No 1107/2009 in accordance with the scientific criteria for the determination of endocrine disrupting properties set out in Commission Delegated Regulation (EU) 2017/2100 and Commission Regulation (EU) 2018/605. The final guidance will be published in the EFSA Journal by July 2018. (07/06/2018)
Guidance on applications for technical equivalence
This Guidance informs potential applicants about their obligations resulting from the provisions of Article 54 of the BPR: when they need to apply for an assessment of technical equivalence and on the procedural steps in making that application. The Guidance also informs potential applicants about the assessment conducted by the Agency and the approach used for assessing the technical equivalence of the alternative source of an active substance versus its reference source. (12/07/2018)
Guidance on active substance suppliers
This Guidance describes the obligations under Article 95 of the BPR and explains the regulatory consequences. (29/03/2017)
Guidance on micro-organisms
This Guidance provides technical advice on the information requirements, the hazard and exposure assessment, the risk characterisation and the evaluation of the active substances and biocidal products in accordance with Annex II, Title 2 and Annex III, Title 2 of the BPR for micro-organisms. (29/03/2017)
ECHA/EFSA guidance on the impact of water treatment processes of residues of active substances in drinking water (08.2023)
The guidance helps you identifying, water residues that require assessment, what water treatment transformation products are formed; and how to conduct a risk assessment that considers consumption of drinking water.